
Vu sur upload.wikimedia.org
mai propriétés physiques. masse molaire : , g/mol; masse volumique : , g/l; température de liquéfaction : ,°c; température de solidification : ,°c
Vu sur pravarini.free.fr
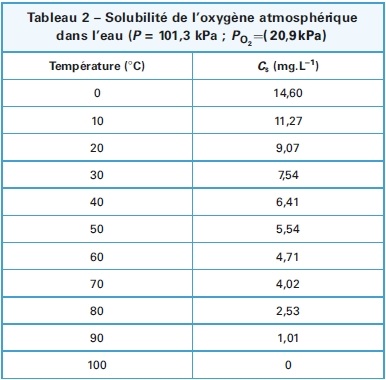
équation : ρ = . . ( ( − t . ) . ) {\displaystyle \rho =. ^{((t )^{.})}} \rho=. ^{((t/ masse volumique du liquide en kmol·m et température en kelvins, de , à , k. valeurs calculées :
Vu sur editions-petiteelisabeth.fr
cette facilité se traduit par des énergies de formation élevées mais, cinétiquement, le dioxygène est souvent peu réactif à température ambiante. ainsi un mélange de dioxygène et de dihydrogène, de fer ou de soufre, etc., n’évolue qu’extrêmement lentement. c’est, en masse, le troisième élément le plus abondant de
air.jpg)
Vu sur pravarini.free.fr
la masse volumique d’une espèce chimique correspond à la masse par une unité de volume de cette espèce. par exemple, suivant l’unité choisie, la masse . pour le dioxygène de masse molaire m = g/mol, ρ= , x soit ρ(dihydrogène) = , g/l. pour le diazote de masse molaire m =

Vu sur editions-petiteelisabeth.fr
masse molaire de o : , g mol. c’est, en masse, le troisième élément le plus abondant de l’univers après l’hydrogène et l’hélium. par ailleurs, le gaz oxygène o sur terre, représente , de la masse de l’air, sous forme de dioxygène o et d’ozone o, soit ,. tonnes environ, (, du volume

Vu sur upload.wikimedia.org
, masse volumique et densité des gaz. . , mettre à jour les cellules. , courtoisenergies, sur fond jaune. , tél : . , conditions normales, conditions. , de temp° et pression, particulières. , température : température : , . °c, . °c. , . k, . k. , pression absolue : pression

Vu sur upload.wikimedia.org
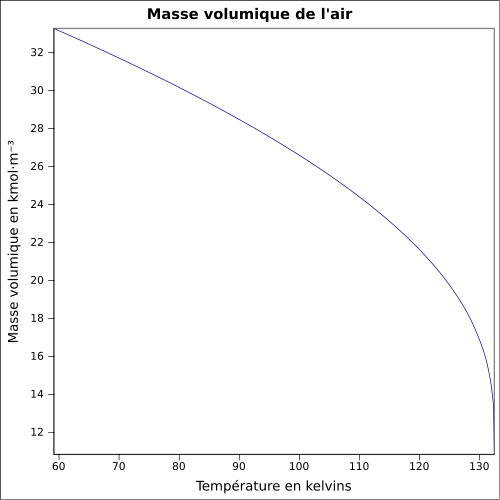
descriptionmasse volumique dioxygène.svg. français : masse volumique calculée d’après : robert h. perry et donald w. green, perry’s chemical engineers’ handbook, mcgrawhill, usa, , e éd., p. (isbn ), p. . date, june . source, own work. author, epop
Vu sur upload.wikimedia.org
dioxygène (n.) .(cismef)Élément gazeux bivalent, incolore, inodore et insipide, qui se trouve à l’état libre dans l’atmosphère, dont il constitue environ un cinquième. numéro atomique : ; masse atomique : ; densité : ,. il se combine avec pratiquement tous les éléments pour former des oxydes. c’est l’agent

Vu sur upload.wikimedia.org
les données statistiques de l’unionpéenne sont exprimées en m, dans les conditions normales (°c, , bar), dans ces conditions la masse volumique du dioxygène est de , kg.m. depuis , la production française est confidentielle. en , la production du japon est de , millions de t. Évolution
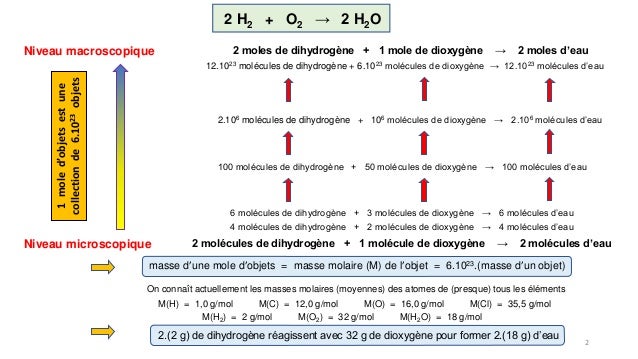
Vu sur image.slidesharecdn.com
, , dihydrogène mol molaire somme unité. ) calculer la masse d’une mole d’air dans les conditions normales de température et de pression ( cntp ) si on considère que l’air est consitué en volume de de dioxygène et de d’azote. masse molaire (g/mol) : n= et o= . ) on définit la densité d’un gaz par







