Élément. symbole. numéro atomique. masse molaire atomique (g.mol). aluminium. al. . , nickel. ni. . ,. or. au. . ,. oxygène. o. . ,. phosphore. p. . ,. plomb. pb. . ,. potassium. k. . ,. silicium. si. . ,. sodium. na. . ,. soufre. s. . ,. strontium. sr. . ,. titane.
Éléments chimiques numéros atomiques masses molaires atomiques (. ) mol.g(. . −. ) nom. symbole. z. masse molaire nom. symbole. z. masse molaire , phosphore. p. . , cadmium. cd. . , platine. pt. . , calcium. ca. . , plomb. pb. . , carbone. c. . , potassium. k. .
coefficient de dilatation à °c = × − k−; Évaluation de la masse volumique du solide: ρ = /(, ⋅(t)) ; avec ρ en kg/m et t en °c; corrélation pour la masse volumique du liquide: ρ = , , ⋅ t ; avec ρ en kg/m et t en °c ; applicable entre et °c; corrélation pour la valeur de cp
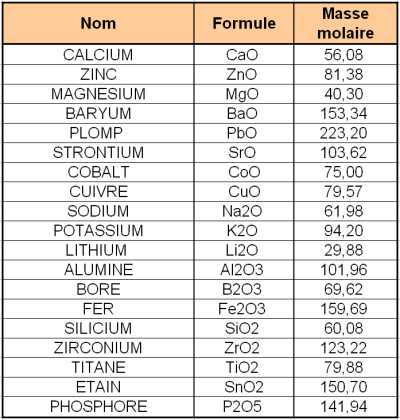
Vu sur sitepasite.free.fr
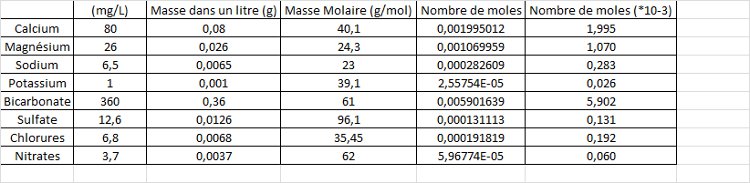
Vu sur ilephysique.net

Vu sur lucad38.files.wordpress.com
masse molaire de l’aluminium al : mal= g/mol. comme il y en a (de al) alors on doit masse molaire du nitrate d’argent : mnirate d’argent=g/mol. masse molaire de l’argent : mag = g/ atomes constituent nbatomes/na = . ▫ = . mol de potassium. masse de potassium : nbmol ▫ mk
la masse molaire et le poids moléculaire de k potassium est .
nom : potassium symbole : k numéro atomique : . masse molaire atomique (g/mol) : approchée plus précise ,. autre nom : chemical abstract service : . etat du corps pur à °c : solide nombre de masse : . nombre de protons : . nombre d’électrons : . nombre de neutrons : . point de

Vu sur upload.wikimedia.org
Vu sur static.intellego.fr

Vu sur patentimages.storage.googleapis.com
hydrogénodiiodate de potassium : fds (fiches de données de sécurité), certificats d’analyse (coa) et de qualité (coq), dossiers, brochures et autres documents disponibles. fds; coa. synonymes: potassium biiodate. numéro ce: formule chimique: kh(io₃)₂ nº cas: masse molaire: .
hydrogénophtalate de potassium : fds (fiches de données de sécurité), certificats d’analyse (coa) et de qualité (coq), dossiers, brochures et autres documents disponibles. fds; coa; notes opératoires. numéro ce: masse molaire: . g/mol grade: reag. ph eur nº cas: formule de hill:
par contre attention de ne pas dire qu’ g de kcl libere g d’ion k, ce serait faux. il faut donc bien calculer la quantité de matière de kcl pour en deduire celle d’ions k. remarque : est la valeur de la masse molaire m atomique du potassium. m(k) = g/mol. tu as besoin de cette valeur mais aussi de
exercice : le potassium (z=) existe sous forme de trois isotopes : k , k et k dont les masses atomiques respectives sont : , ; , ; , u.m.a . l’isotope k est le plus rare, son abondance naturelle est de , . sachant que la masse molaire du potassium naturel est , u.m.a, calculer les
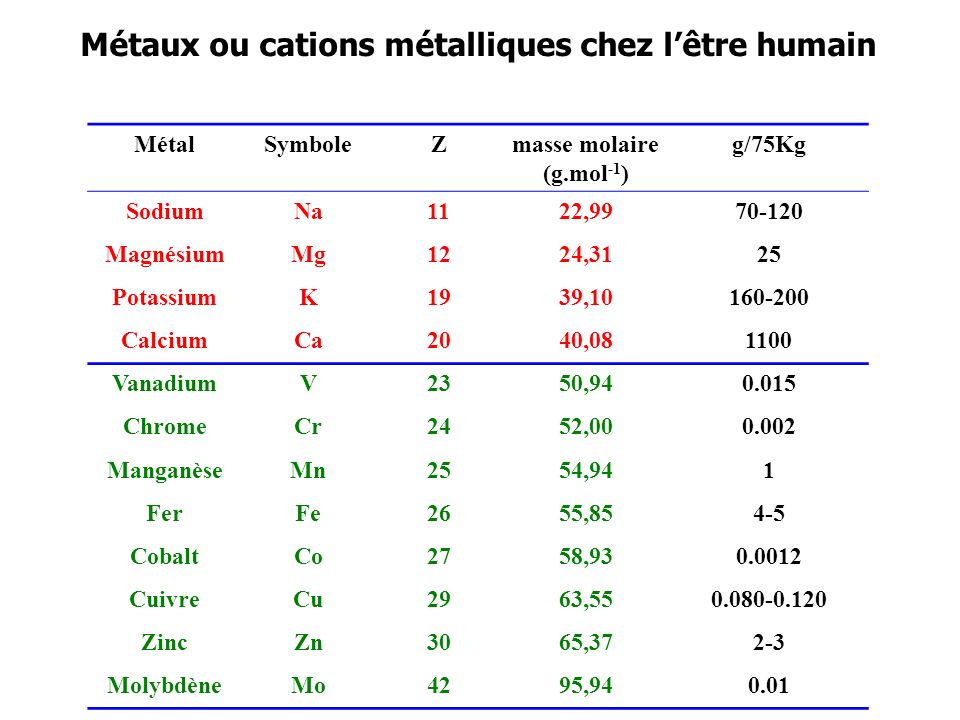
Vu sur slideplayer.fr

Vu sur docplayer.fr

Vu sur slideplayer.fr

Vu sur sitepasite.free.fr








